| Bio-Ecke | Chemie-Ecke | Home | Unterricht | sOWLrebel |
|---|
Wõhrend zur Herstellung von Nitrobenzol konzentrierte Salpetersõure und konzentrierte Schwefelsõure bei 60░C einwirken m³ssen, gelingt
die Nitrierung von Phenol bereits mit 25 %iger Salpetersõure bei RT.
Eine derartige Aktivierung des aromatischen Ringes bewirken neben der Hydroxylgruppe auch die Methylgruppe (Methylbenzol, Toluol)
und die Aminogruppe (Anilin).
Umgekehrt verringert die Nitrogruppe die Neigung zu einer Zweitsubstitution. Nitrobenzol lõsst sich nur mit einem Gemisch aus rauchender
Salpetersõure und konzentrierter Schwefelsõure und bei Temperaturen von ³ber 90░C weiter nitrieren.
Die Nitrogruppe (-NO2), aber auch die Gruppen ¢CN, -SO3H, -CHO, -COOH und ¢Halogene desaktivieren
den aromatischen Ring.
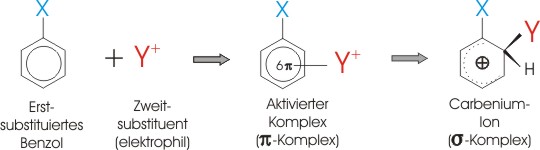
Erstsubstituenten verõndern nicht nur die Reaktivitõt. Sie bewirken zudem, dass der Zweitsubstituent in einer ganz bestimmten Orientierung zum Erstsubstituenten eingebaut wird.
Wõhrend sich bei einer gleich hõufigen Substitution an allen f³nf zur Verf³gung stehenden Positionen des Ausgangsstoffes C6H5-X das Produkt zu je 2/5 aus dem ortho- und dem meta-Isomeren und zu 1/5 aus dem para-Isomeren zusammensetzen m³sste, ist das tatsõchliche Reaktionsverhalten ganz anders.
Es gibt Erstsubstituenten (-OH, -CH3, -Halogene), die den Zweitsubstituenten bevorzugt in o- und p- Stellung dirigieren, und Substituenten (-NO2, -CN, -SO3H. -CHO, -COOH), die eine weitere Substitution in m- Stellung beg³nstigen.
|
aktivierend |
ortho-, para- dirigierend |
-OH, -CH3, -NH2 |
|
desaktivierend |
meta- dirigierend ortho-, para- dirigierend |
-NO2,
-CN, -SO3H, -CHO, -COOH -Halogene |
Auftreten von ortho-, meta-, para- Isomeren bei der Nitrierung eines bereits substituierten Benzols:
|
|
ortho- (%) |
para- (%) |
Summe o- + p- |
meta- (%) |
|
-OH |
~50 |
~50 |
100% |
Spuren |
|
-CH3 |
59 |
37 |
96 |
4 |
|
-Cl |
30 |
70 |
100 |
Spuren |
|
-Br |
37 |
62 |
99 |
1 |
|
-NO2 |
6 |
< 1 |
7 |
93 |
|
-CN |
|
|
19 |
81 |
|
-SO3H |
21 |
7 |
28 |
72 |
|
-CHO |
|
|
28 |
72 |
|
-COOH |
19 |
1 |
20 |
80 |
▄ber die Reaktivitõt entscheidet daher wie leicht sich der pi-Komplex bildet.
Wird dieser aktivierte Komplex durch einen Substituenten stabilisiert und somit die notwendige
Aktivierungsenergie verringert, so nimmt die Reaktivitõt zu.
Da die Energien der aktivierten Komplexe aber nur schwer abzuschõtzen sind, verwendet man meist die
Energien der Zwischenstoffe (Carbeniumionen), die nahe an den Energien der ▄bergangszustõnde liegen.
Das stabilste Carbeniumion erfordert zu seiner Bildung die geringste Aktivierungsenergie.

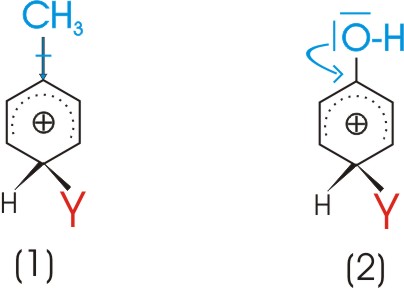
Stabilisierung durch Elektronendonatoren:
Das Carbeniumion ist umso stabiler, je mehr seine positive Ladung abgeschwõcht wird. Eine Verringerung
der positiven Ladung des Ions kann durch einen elektronenliefernden Erstsubstituenten
(blau) bewirkt werden.
Als Elektronendonatoren sind m÷glich:
1) Substituenten mit einem positiven induktiven Effekt (+I-Effekt), die die gemeinsame Elektronenwolke zum Ring verschieben
2) Substituenten mit einem positiven Mesomerieeffekt (+M-Effekt), die ein freies Elektronenpaar dem Ring zur Verf³gung stellen.
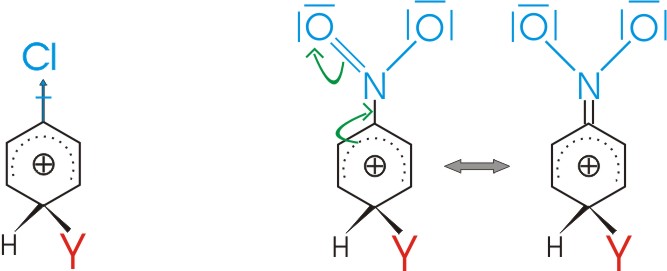
Erschwerte Bildung durch Elektronenakzeptoren:
Umgekehrt wird ein Substituent mit negativ induktivem Effekt (-I-Effekt) oder mit einem negativen Mesomerieeffekt (-M-Effekt) die positive Ladung des Carbeniumions noch erh÷hen und damit eine weitere Substitution erschweren (Elektronenakzeptoren):
Es werden hauptsõchlich diejenigen Vorgõnge ablaufen, die die geringste Aktivierungsenergie ben÷tigen.
Ein sigma-Komplex (Carbeniumion) ist umso stabiler (= niedrigste Energie), je mehr positive Ladungen
delokalisiert sind.
Um die dirigierende Wirkung von Substituenten zu verstehen, muss man ihren Einfluss auf die bei
o-, m- und p- Substitution gebildeten Carbeniumionen betrachten.
Ohne Erstsubstitution lõsst sich das Carbeniumion durch folgende Grenzformeln veranschaulichen:
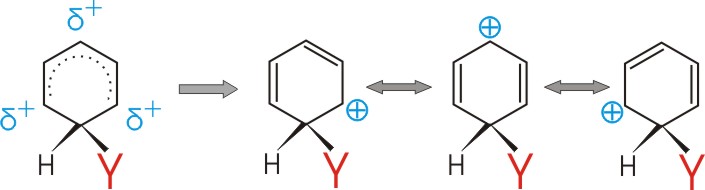
In o- und p- Stellung zum neu eintretenden (Zweit-)Substituenten (Y) treten positive Partialladungen auf.
In m-Stellung befindet sich keine positive Partialladung!!!!!
Diese Ladungsverteilung wird durch verschiedenen Erstsubstituenten (X) in unterschiedlicher Weise beeinflusst:
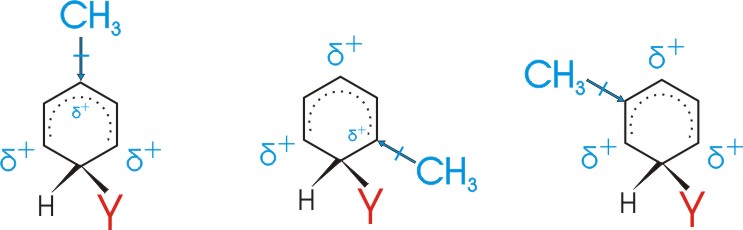
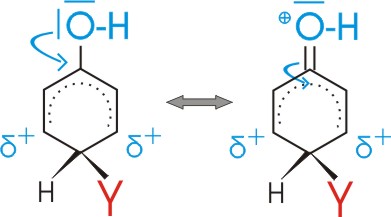
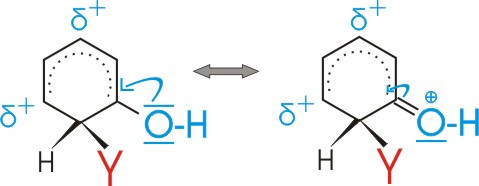
Substituenten mit +I oder +M Effekt erniedrigen also die Energie des sigma-Komplexes f³r den Fall der o- und p- Substitution
--> o- und p- Substitutionsprodukte bilden sich daher schneller.
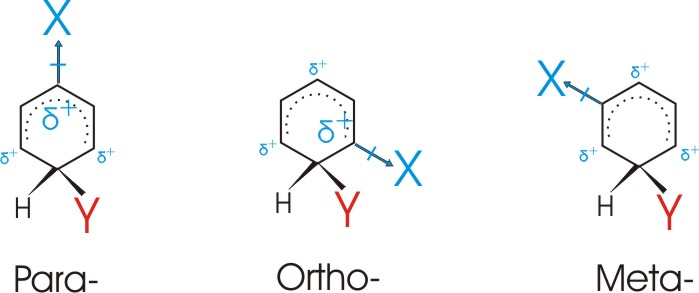
Hier sind sowohl ¢I als auch +M Effekt wirksam.
Als Folge des ¢I Effekts ist die Substitutionsgeschwindigkeit erniedrigt, er reicht allerdings nicht aus, um den
+M Effekt zu kompensieren.
|
Erstsubstituent mit |
Wirkung auf
Zweitsubstituenten |
Dirigieren des
Zweitsubstituenten |
Beispiele |
|
+M |
aktivierend |
o- und p- Stellung |
-OH, -OCH3, -HN2 |
|
+I |
(weniger) aktivierend |
o- und p- Stellung |
-CH3, -Alkylrest |
|
-M oder ¢I |
desaktivierend |
m- Stellung |
-NO2, -COH, -COOH |
|
-I und +M |
desaktivierend (wegen ¢I) |
o- und p- Stellung (wegen +M) |
-Halogene |